- Delovanje: avtomatsko, krmiljeno s PLC
- Pripomočki: Za proizvodnjo 1.000 Nm³/h H2od zemeljskega plina so potrebne naslednje naprave:
- 380-420 Nm³/h zemeljski plin
- 900 kg/h napajalne vode kotla
- 28 kW električne moči
- 38 m³/h hladilne vode *
- * se lahko nadomesti z zračnim hlajenjem
- Stranski proizvod: izvoz pare, če je potrebno
Video
Proizvodnja vodika iz zemeljskega plina je izvajanje kemijske reakcije stisnjenega in razžvepljenega zemeljskega plina in pare v posebnem reformerju, polnjenem s katalizatorjem, in ustvarjanje reforming plina s H₂, CO₂ in CO, pretvorba CO v reforming plinih v CO₂ in nato ekstrakcija kvalificiranega H₂ iz reforming plinov z adsorpcijo z nihanjem tlaka (PSA).
Zasnova obrata za proizvodnjo vodika in izbira opreme izhajata iz obsežnih inženirskih študij TCWY in ocen prodajalcev, pri čemer je še posebej optimizirano naslednje:
1. Varnost in enostavnost delovanja
2. Zanesljivost
3. Kratka dobava opreme
4. Minimalno terensko delo
5. Konkurenčni kapitalski in operativni stroški
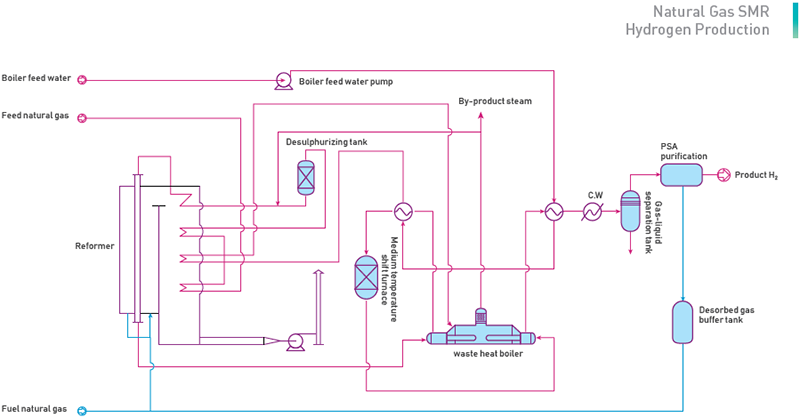
(1) Razžveplanje zemeljskega plina
Pri določeni temperaturi in tlaku z dovodnim plinom z oksidacijo adsorbenta mangana in cinkovega oksida bo skupno žveplo v dovodnem plinu padlo pod 0,2 ppm, da bi izpolnili zahteve katalizatorjev za parno reformo.
Glavna reakcija je:
| COS+MnO |
| MnS+H2O |
| H2S+ZnO |
(2) Parno reformiranje NG
Postopek parnega reformiranja uporablja vodno paro kot oksidant, z nikljevim katalizatorjem pa bodo ogljikovodiki reformirani v surovi plin za proizvodnjo vodikovega plina. Ta proces je endotermni proces, ki zahteva dovod toplote iz sevalnega dela peči.
Glavna reakcija v prisotnosti nikljevih katalizatorjev je naslednja:
| CnHm+nH2O = nCO+(n+m/2)H2 |
| CO+H2O = CO2+H2 △H°298= – 41KJ/mol |
| CO+3H2 = CH4+H2O △H°298= – 206KJ/mol |
(3) Čiščenje PSA
Kot proces kemične enote se tehnologija ločevanja plinov PSA hitro razvija v neodvisno disciplino in se vedno bolj uporablja na področjih petrokemične, kemijske, metalurške industrije, elektronike, nacionalne obrambe, medicine, lahke industrije, kmetijstva in varstva okolja. industrije itd. Trenutno je PSA postal glavni proces H2ločevanje, ki se uspešno uporablja za čiščenje in ločevanje ogljikovega dioksida, ogljikovega monoksida, dušika, kisika, metana in drugih industrijskih plinov.
Študija ugotavlja, da lahko nekateri trdni materiali z dobro porozno strukturo absorbirajo molekule tekočine in takšen vpojni material imenujemo absorbent. Ko molekule tekočine pridejo v stik s trdnimi adsorbenti, pride do adsorpcije takoj. Posledica adsorpcije je različna koncentracija absorbiranih molekul v tekočini in na vpojni površini. Molekule, ki jih adsorbira absorbent, bodo obogatene na njegovi površini. Kot običajno bodo različne molekule pokazale različne lastnosti, ko jih bodo absorbirali adsorbenti. Na to bodo neposredno vplivali tudi zunanji pogoji, kot sta temperatura tekočine in koncentracija(tlak). Zato lahko ravno zaradi tovrstnih različnih lastnosti s spremembo temperature ali tlaka dosežemo separacijo in čiščenje zmesi.
Za to napravo so v adsorpcijsko posteljo napolnjeni različni adsorbenti. Ko reforming plin (plinska mešanica) teče v adsorpcijsko kolono (adsorpcijsko plast) pod določenim tlakom, zaradi različnih adsorpcijskih značilnosti H2, CO, CH2, CO2, itd. CO, CH2in CO2adsorbirajo adsorbenti, H2bo iztekel z vrha postelje, da bo dobil kvalificiran produkt vodik.










 MnS+CO2
MnS+CO2









